martes, 2 de marzo de 2010
AIRE ACONDICIONADO
Es el proceso más completo de tratamiento del aire ambiente de los locales habitados; consiste en regular las condiciones en cuanto a la temperatura (calefacción o refrigeración), humedad, limpieza (renovación, filtrado) y el movimiento del aire dentro de los locales. Si no se trata la humedad, sino solamente de la temperatura, podría llamarse climatización
HISTORIA DEL AIRE ACONDICIÓNADO
ž En la antigüedad, los egipcios ya utilizaban sistemas y métodos para reducir el calor. Se utilizaba principalmente en el palacio del faraón, cuyas paredes estaban formadas por enormes bloques de piedra, con un peso superior a mil toneladas. Durante la noche, tres mil esclavos desmantelaban las paredes y acarreaban las piedras al Desierto del Sahara. Como el clima desértico es extremoso y la temperatura disminuye a niveles muy bajos durante las horas nocturnas, las piedras se enfriaban notablemente y antes del amanecer los esclavos acarreaban de regreso las piedras al palacio para colocarlas en su sitio. Así el faraón disfrutaba de temperaturas alrededor de los 26° Celsius, mientras que afuera el calor subía hasta casi el doble.
ž También buscaban guardad alimentos en pozos hechos por los hombres cercas de los ríos y por la humedad que rodea siempre a esos lugares estos permanecían frescos ahí cerca del rio.
PRINCIPIOS DEL AIRE ACONDICIÓNADO
ž En 1842, Lord Kelvin inventó el principio del aire acondicionado. Con el objetivo de conseguir un ambiente agradable y sano, el científico creó un circuito frigorífico hermético basado en la absorción del calor a través de un gas refrigerante. Para ello, se basó en 3 principios:
El calor se transmite de la temperatura más alta a la más baja, como cuando enfriamos un café introduciendo una cuchara de metal a la taza y ésta absorbe el calor.
El cambio de estado del líquido a gas absorbe calor. Por ejemplo, si humedecemos la mano en alcohol, sentimos frío en el momento en que éste se evapora, puesto que absorbe el calor de nuestra mano.
La presión y la temperatura están directamente relacionadas. En un recipiente cerrado, como una olla, necesitamos proporcionar menor cantidad de calor para llegar a la misma temperatura que en uno abierto.
PRINCIPIOS DEL AIRE ACONDICIÓNADO
En 1902, el estadounidense Willis Haviland Carrier sentó las bases de la refrigeración moderna y, al encontrarse con los problemas de la excesiva humidificación del aire enfriado, las del aire acondicionado, desarrollando el concepto de climatización de verano.
Carrier graduado de la universidad y con maestría en ingeniería se puso a investigar con tenacidad cómo resolver el problema y diseñó una máquina que controlaba la temperatura y la humedad por medio de tubos enfriados, dando lugar a la primera unidad de aire acondicionado de la Historia. Esto con la intención de solucionar el problema de un impresor de Brooklyn N:Y que tenia problemas por la temperatura del ambiente durante el proceso de impresión.Aunque Willis Haviland Carrier es reconocido como el “padre del aire acondicionado”, el término “aire acondicionado” fue utilizado por primera vez por el ingeniero Stuart H. Cramer, en la patente.
FUNCIONAMIENTO DEL AIRE ACONDICIÓNADO
ž El compresor, el cual se encuentra en la unidad exterior, aspira el gas refrigerante y lo comprime. Debido a esta compresión el gas refrigerante se calienta aun más de lo que ya estaba, aumenta su presión y con la presión aumenta la temperatura de condensación del gas refrigerante (temperatura que hace falta para convertir el gas refrigerante en líquido refrigerante). Ahora el compresor bombea este gas refrigerante caliente al condensador donde este gas es enfriado por un ventilador, que sopla aire exterior por encima de las láminas del condensador.
ž El líquido refrigerante traspasa por una válvula reductora al evaporador en la unidad interior. La válvula reductora cambia la presión del líquido refrigerante reduciéndo presión en la unidad interior.
COMPONENTES ESENCIALES DE UN CLIMA
ž Abanico.
ž Compresor.
ž Termómetro.
ž Líquido enfriador.
ž Panel o condensador.
ž Las funciones que deben cumplir los equipos de aires acondicionados consisten en
En verano: enfriamiento y de humectación.
En invierno: calentamiento y humectación.
Comunes en invierno y verano: ventilación, filtrado y circulación.
Para conseguir ese efecto halló los siguientes principios
Que el calor se transmita de la temperatura más alta a la más baja,
que el cambio de estado de líquido a gaseoso absorbe calor,
y que la presión y la temperatura están directamente relacionadas.
ž Estos procesos deben realizarse
v Automáticamente.
v Sin ruidos molestos.
v Con el menor consumo energético.
domingo, 28 de febrero de 2010
ISOTERMA Y MAS
Isoterma Es una que une los puntos, en un plano cartográfico, que presentan las mismas temperaturas en la unidad de tiempo considerada. Así, para una misma área, se pueden diseñar un gran número de planos con isotermas, describe las relaciones Presion-Volumen a temperatura constante en el caso de los gases.En general es isoterma o isotermico mejor dicho todo aquello que sucede a temperatura constante (iso=igual, termo=temperatura).Como el estado de la materia se puede describir con tres variables y las mas comunes son P, V y T, si se fija T queda una relacion entre P y V y esa relacion se puede graficar en el plano (dos variables) con lo que se obtiene una curva que se llama "isoterma".
Ejemplo: Isotermas de la temperatura media de largo periodo del mes de enero, de febrero, etc., o las isotermas de las temperaturas medias anuales.
PROCESO ISOMETRICO
Proceso isométrico o Isocórico: durante este proceso el volumen es constante, el gas absorbe una cantidad de calor, aumentando por ende su temperatura hasta un valor final o en caso contrario; un gas se enfría desde una temperatura inicial hasta una temperatura final manteniendo su volumen constante y disipando una cantidad de calor. W=0Un proceso que se efectúa a volumen constante sin que haya ningún desplazamiento, el trabajo hecho por el sistema es cero. Es decir, en un proceso isocórico no hay trabajo realizando por el sistema. Y no se adiciona calor al sistema que ocasione un incremento de su energía interna.
Ejemplo: El proceso térmico que se desarrolla en una olla presión de uso doméstico, desde el momento que se coloca al fuego hasta que escapa por primera vez aire a través de la válvula, corresponde a un proceso a volumen constante.
PROCESO ADIABATICO
En termodinámica se designa como proceso adiabático a aquél en el cual el sistema (generalmente, un fluido que realiza un trabajo) no intercambia calor con su entorno. Un proceso adiabático que es además reversible se conoce como proceso isentrópico. El extremo opuesto, en el que tiene lugar la máxima transferencia de calor, causando que la temperatura permanezca constante, se denomina como proceso isotérmico.El término adiabático hace referencia a elementos que impiden la transferencia de calor con el entorno.
Ejemplo: Una pared aislada se aproxima bastante a un límite adiabático. Otro ejemplo es la temperatura adiabática de llama, que es la temperatura que podría alcanzar una llama si no hubiera pérdida de calor hacia el entorno.
ENTROPIA
La entropía describe lo irreversible de los sistemas termodinámicos. En termodinámica, la entropía (simbolizada como S) es la magnitud física que mide la parte de la energía que no puede utilizarse para producir trabajo. Es una función de estado de carácter extensivo y su valor, en un sistema aislado, crece en el transcurso de un proceso que se dé de forma natural. La palabra entropía procede del griego y significa evolución o transformación. Fue Rudolf Clausius quien le dio nombre y la desarrolló durante la década de 1850.
miércoles, 27 de enero de 2010
CONVECCION, RADIACION TERMICA, CONDENSACION Y PUNTO DE FUSION
El punto de fusión es la temperatura a la cual la materia pasa de estado sólido a estado líquido.
El punto de fusión de una sustancia pura es siempre más alto y tiene una gama más pequeña que el punto de fusión de una sustancia impura. Cuanto más impuro sea, más bajo es el punto de fusión y más amplia es la gama. Eventualmente, se alcanza un punto de fusión mínimo. El cociente de la mezcla que da lugar al punto de fusión posible más bajo se conoce como el punto eutéctico.

Se denomina condensación al cambio de estado de la materia que se encuentra en forma gaseosa a forma líquida. Es el proceso inverso a la vaporización. Si se produce un paso de estado gaseoso a estado sólido de manera directa, el proceso es llamado sublimación inversa.

Se denomina radiación térmica o radiación calorífica a la emitida por un cuerpo debido a su temperatura. Todos los cuerpos con temperatura superior a 0 K emiten radiación electromagnética, siendo su intensidad dependiente de la temperatura y de la longitud de onda considerada. En lo que respecta a la transferencia de calor la radiación relevante es la comprendida en el rango de longitudes de onda de 0,1µm a 100µm, abarcando por tanto parte de la región ultravioleta, la visible y la infrarroja del espectro electromagnético.

La convección es una de las tres formas de transferencia de calor y se caracteriza porque se produce por intermedio de un fluido (aire, agua) que transporta el calor entre zonas con diferentes temperaturas. La convección se produce únicamente por medio de materiales fluidos. Éstos, al calentarse, aumentan de volumen y, por lo tanto, disminuyen su densidad y ascienden desplazando el fluido que se encuentra en la parte superior y que está a menor temperatura. Lo que se llama convección en sí, es el transporte de calor por medio de las corrientes ascendente y descendente del fluido.
La transferencia de calor implica el transporte de calor en un volumen y la mezcla de elementos macroscópicos de porciones calientes y frías de un gas o un líquido. Se incluye también el intercambio de energía entre una superficie sólida y un fluido o por medio de una bomba, un ventilador u otro dispositivo mecánico (convección mecánica o asistida).
miércoles, 20 de enero de 2010
TAREAS DE INVESTIGACION
La Ley de Charles y Gay-Lussac, también llamada Ley de Charles explica las leyes de los gases ideales. Relaciona el volumen y la temperatura de una cierta cantidad de gas ideal, mantenido a una presión constante, mediante una constante de proporcionalidad directa. En esta ley, Charles dice que a una presión constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura el volumen del gas disminuye. Esto se debe a que "temperatura" significa movimiento de las partículas. Así que, a mayor movimiento de las partículas (temperatura), mayor volumen del gas.
La ley fue publicada primero por Louis Joseph Gay-Lussac en 1802, pero hacía referencia al trabajo no publicado de Jacques Charles, de alrededor de 1787, lo que condujo a que la ley sea usualmente atribuida a Charles. La relación había sido anticipada anteriormente en los trabajos de Guillaume Amontons en 1702.
Por otro lado, Gay Lussac relacionó la presión y la temperatura como unidades directamente proporcionales y es llamada "La segunda ley de Gay-Lussac"
Expresión algebraica:
La ley de Charles es una de las más importantes leyes acerca del comportamiento de los gases, y ha sido usada de muchas formas diferentes, desde globos de aire caliente hasta acuarios. Se expresa por la fórmula:en esta ley actúan la presión de un gas ideal así como la de un gas constante.
Despejando V1 se obtiene:
Despejando V2 se obtiene:
donde:
V es el volumen
T es la temperatura absoluta (es decir, medida en Kelvin)
k es la constante de proporcionalidad
De Wikipedia, la enciclopedia libre
Saltar a navegación, búsqueda
La Ley de Boyle-Mariotte (o Ley de Boyle), formulada por Robert Boyle y Edme Mariotte, es una de las leyes de los gases ideales que relaciona el volumen y la presión de una cierta cantidad de gas mantenida a temperatura constante. La ley dice que el volumen es inversamente proporcional a la presión:
donde es constante si la temperatura y la masa del gas permanecen constantes.
Cuando aumenta la presión, el volumen disminuye, mientras que si la presión disminuye el volumen aumenta. El valor exacto de la constante k no es necesario conocerlo para poder hacer uso de la Ley; si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:

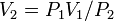
P1= Presión Inicial
P2= Presión Final
V1= Volumen Inicial
V2= Volumen Final

Junto con la ley de Charles y Gay-Lussac y la ley de Graham, la ley de Boyle forma las leyes de los gases, que describen la conducta de un gas ideal. Las tres leyes pueden ser generalizadas en la ecuación universal de los gases.
Ley de Graham
La Ley de Graham, formulada en 1829 por Thomas Graham, establece que las velocidades de difusión de los gases son inversamente proporcionales a las raíces cuadradas de sus respectivas densidades.
Gráficamente:
Siendo v las velocidades y δ las densidades.
Se hace uso de este principio en el método de difusión de separación de isótopos.
Los diferentes procesos que se realizan en las plantas, como lo son: la difusión, la osmosis y la imbibición. se encuentran íntimamente ligados con el transporte de agua y de soluciones desde el punto de origen hasta el medio donde esta es activada. Cada sustancia se difunde libremente de otras hasta que se difunden todas equitativamente. En la planta la velocidad de difusión depende del gradiente lo cual esta determinado por la diferencia entre las concentraciones de las sustancias en las dos regiones y por la distancia que las separa. El fenómeno de difusión esta relacionado con la energía cinética de las moléculas. gracias a su movimiento constante, las partículas de una sustancia, se distribuyen uniformemente en el espacio libre. Si hay una concentración mayor de partículas en un punto habrá más choques entre sí, por lo que hará que se muevan hacia las regiones de menor número: las sustancias se difunden de una región de mayor concentración a una región de menor concentración.
Velocidad de difusión de los gases
De los 4 estados de la materia, los gases presentan la mayor facilidad de difusión de sus respectivas moléculas, como ocurre en el aire, ya que sus moléculas tienen velocidades superiores. Las moléculas de diferentes clases tienen velocidades diferentes, a temperatura constante, dependiendo únicamente de la densidad.
Ejemplo
¿cual es la velocidad de difusión del oxígeno con respecto al hidrógeno? si la masa molar del oxígeno es 16 y la del hidrógeno es 1:
La velocidad de difusión del hidrógeno es 4 veces mayor que la del oxígeno.
La presión absoluta se mide con relación al cero absoluto o vacío total.
La presión relativa se mide con respecto a la presión atmosférica, es decir, su valor cero corresponderá al valor de la presión absoluta atmosférica.
La presión atmosférica es la que ejerce la masa de aire de la atmósfera terrestre sobre su superficie, medida mediante un barómetro. A nivel del mar, la presión atmosférica es de aproximadamente 760 mm de Hg absolutos, que es equivalente a 14,7 psia.
Otro tipo de medida de esta variable, frecuentemente usada es la presión diferencial, que consistirá en la medida de la misma entre dos puntos de un proceso.
La presión de vacío es aquella que se mide como la diferencia entre una presión atmosférica y la presión absoluta (cero absoluto).
Presión manometrica. Es la presión medida con referencia a la presión atmosférica la diferencia entre la presión medida y la presión atmosférica real. Como ésta es variable, la comparación de valores medidos en diferentes intervalos de tiempo, resulta incierta.
Presión hidrostatica. Es la presión existente bajo la superficie de un líquido, ejercida por el mismo.
Presión de línea. Es la fuerza ejercida por el fluido, por unidad de superficie, sobre las paredes de una conducción por la que circula.
Presión diferencial. Es la diferencia entre un determinado valor de presión y otro utilizado como referencia. En cierto sentido, la presión absoluta podría considerarse como una presión diferencial que toma como referencia el vacío absoluto, y la presión manométrica como otra presión diferencial que toma como referencia la presión atmosférica.
Los elementos primarios de medición de presión son fundamentalmente de tres tipos:
1.- Elementos Mecánicos

 William Thomson Lord Kelvin Matemático y físico británico Nació el 26 de junio de 1824 en Belfast. Cursó estudios en las universidades de Glasgow y Cambridge. Entre 1846 y 1899 trabajó como profesor de la Universidad de Glasgow. En termodinámica, desarrolló el trabajo realizado por James Prescott Joule sobre la interrelación del calor y la energía mecánica, y en 1852 ambos unieron esfuerzos en la investigación del fenómeno al que se conoció como efecto Joule-Thomson. En 1848 estableció la escala absoluta de temperatura que sigue llevando su nombre. Estudió la teoría matemática de la electrostática, llevó a cabo mejoras en la fabricación de cables e inventó el galvanómetro de imán móvil y el sifón registrador. Fue asesor científico en el tendido de cables telegráficos del Atlántico en 1857, 1858, 1865 y 1866. Además contribuyó a la teoría de la elasticidad e investigó los circuitos oscilantes, las propiedades electrodinámicas de los metales y el tratamiento matemático del magnetismo. Junto con el fisiólogo y físico alemán Hermann Ludwig von Helmholtz, hizo una estimación de la edad del Sol y calculó la energía irradiada desde su superficie. Entre los aparatos que inventó o mejoró se encuentran un dispositivo para predecir mareas, un analizador armónico y un aparato para grabar sonidos en aguas más o menos profundas. También mejoró aspectos de la brújula marina o compás náutico. En 1902, elabora el primer modelo atómico. Muchas de sus obras científicas se recopilaron en su Ponencias sobre electricidad y magnetismo (1872), Ponencias matemáticas y físicas (1882, 1883, 1890) y Cursos y conferencias (1889-1894). Fue presidente de la Sociedad Real de Londres en 1890, y en 1902 recibió la Orden del Mérito. Falleció el 17 de diciembre de 1907.
William Thomson Lord Kelvin Matemático y físico británico Nació el 26 de junio de 1824 en Belfast. Cursó estudios en las universidades de Glasgow y Cambridge. Entre 1846 y 1899 trabajó como profesor de la Universidad de Glasgow. En termodinámica, desarrolló el trabajo realizado por James Prescott Joule sobre la interrelación del calor y la energía mecánica, y en 1852 ambos unieron esfuerzos en la investigación del fenómeno al que se conoció como efecto Joule-Thomson. En 1848 estableció la escala absoluta de temperatura que sigue llevando su nombre. Estudió la teoría matemática de la electrostática, llevó a cabo mejoras en la fabricación de cables e inventó el galvanómetro de imán móvil y el sifón registrador. Fue asesor científico en el tendido de cables telegráficos del Atlántico en 1857, 1858, 1865 y 1866. Además contribuyó a la teoría de la elasticidad e investigó los circuitos oscilantes, las propiedades electrodinámicas de los metales y el tratamiento matemático del magnetismo. Junto con el fisiólogo y físico alemán Hermann Ludwig von Helmholtz, hizo una estimación de la edad del Sol y calculó la energía irradiada desde su superficie. Entre los aparatos que inventó o mejoró se encuentran un dispositivo para predecir mareas, un analizador armónico y un aparato para grabar sonidos en aguas más o menos profundas. También mejoró aspectos de la brújula marina o compás náutico. En 1902, elabora el primer modelo atómico. Muchas de sus obras científicas se recopilaron en su Ponencias sobre electricidad y magnetismo (1872), Ponencias matemáticas y físicas (1882, 1883, 1890) y Cursos y conferencias (1889-1894). Fue presidente de la Sociedad Real de Londres en 1890, y en 1902 recibió la Orden del Mérito. Falleció el 17 de diciembre de 1907. Daniel Gabriel Fahrenheit nació en Danzig, Gdansk (actual Polonia) un 24 de mayo de 1686. Importante físico del cual se tomó el nombre para la escala Fahrenheit de temperatura.
Daniel Gabriel Fahrenheit nació en Danzig, Gdansk (actual Polonia) un 24 de mayo de 1686. Importante físico del cual se tomó el nombre para la escala Fahrenheit de temperatura.Recordado autor de numerosos inventos, entre los que cabe citar, en 1709 los termómetros de agua, de mercurio en 1714, y el diseño de la escala termométrica.
Si bien fue de origen alemán, Fahrenheit, ha permanecido la mayor parte de su vida en Holanda.
A sus 15 años de edad, tras el fallecimiento de sus padres, se mudó a Ámsterdam, ciudad que captó notablemente su atención debido que era uno de los centros más activos de la fabricación de instrumentos científicos.
Fue a esa corta edad, que comenzó a trabajar como soplador de vidrio a construir instrumentos científicos de precisión, conociéndo a Roemer en ese tiempo.
Fahrenheit dejó su firma en la historia mundial, tras el diseño de una escala, que empleaba como referencia una mezcla de agua y sal en partes iguales, cuya temperatura de congelación es más baja que la del agua y la de ebullición más alta.
Estableció como valores de congelación y ebullición del agua convencional el "0" y el "100" de la escala Celsius, los cuales, con sus aportes, han quedado fijados en 32 °F y 212 °F, respectivamente.
La escala Fahrenheit ha permitido mayor precisión que la centígrada a la hora de delimitar una temperatura determinada, diciendo que 180 grados Fahrenheit corresponden a 100 grados Celsius.
1714 Daniel publicó estos resultados en el "Acta Editorum", y sorprendió con las sustitución del líguido de referencia en los termómetros, el alcohol en el momento (a partir de los conocimientos que había adquirido Roemer de la expansión térmica de los metales) ubicando al mercurio como nueva referencia, y luego de inventar un método de purificación del mismo para que no se pegara en las paredes del termómetro.
1724 Gracias a su gran conocimiento por los trabajos de otros científicos, publicó los suyos propios en las "Philosophical Transactions" de la Royal Society
Mientras que el Grado Celsius se define con la evaporación y ebullición del agua, el grado Fahrenheit lo hace con Cloruro amónico.
Tras su muerte, el 16 de Septiembre de 1736, y en su honor, se decide unificar su escala termométrica, tomando como referencia 213 grados para la temperatura de ebullición del agua y 98,6 en vez de 96 para la correspondiente al cuerpo humano.
 Anders Celsius, físico y astrónomo sueco, nació en Ovanåker, Suecia, en el año 1701.
Anders Celsius, físico y astrónomo sueco, nació en Ovanåker, Suecia, en el año 1701.Este hombre se ha identificado siempre por su sabiduría, la vida que ha llevado y el invento que ha dejado en nuestra historia.El ha sido en sus comienzos profesor de astronomía en la Universidad de Uppsala, precisamente en el año 1730, y luego ha supervisado la construcción del Observatorio de la misma ciudad, del que más adelante es nombrado director.
Además tres años más tarde, Anders ha publicado una colección de 316 observaciones de auroras boreales, sumado a su participación en una expedición a Laponia para medir un arco de meridiano terrestre, lo cual confirma la teoría de Isaac Newton de que la Tierra se achataba en los polos.
Tal es así, que se presenta en una memoria en la Academia de Ciencias Sueca, en la que propone la escala centígrada de temperaturas, conocida posteriormente como Escala Celsius.
Celsius es reconocido en mayor pocentaje, por habernos dejado tal invento útil en la sociedad, como ha sido la escala centesimal del termómetro. Este instrumento durante el siglo XVI era graduado como "frío" colocándolo en una cueva y "caliente" exponiéndolo a los rayos del sol estival o sobre la piel caliente de una persona, hasta que Réaumur y Farenheit lo graduaron basándose en la temperatura del hielo en su punto de fusión y en la del vapor de agua al hervir.
Por tal motivo variaban según su país natal, como ha sido establecido en la escala alemana de 32 a 212 grados, mientras que la francesa lo hacía de 0 a 80 grados.
Es en el año 1742, cuando Celsius propone sustituir la escala del científico alemán por otra cuyo manejo era más sencillo, y por supuesto más conveniente, una escala centesimal que iba de 0 a 100 grados. En esta escala, el punto correspondiente a la temperatura 0ºC coincidía con el punto de congelación del agua, mientras que la temperatura a 100ºC equivalía a la temperatura de ebullición del agua a nivel del mar. Esta, por lo tanto, indicaba un descenso de temperatura cuando el calor aumentaba, al contrario de como es conocida actualmente.
La escala centígrada de temperaturas ha sido propuesta en una memoria que presentó a la Academia de Ciencias Sueca, y así el Termómetro de Celsius se hace sumamente conocido durante años como "termómetro sueco" por la comunidad científica, y tan sólo se popularizó el nombre de "termómetro Celsius" a partir del S. XIX.














